Inhalatorbehandling
Magnus Svartengren, professor
Yrkes- och miljömedicin, Karolinska Institutet, Solna
Martin Anderson, överläkare
Fysiologiska kliniken, SÖS
Den första dosaerosolen kom 1956. Den var en liten trycksatt behållare som levererar en spraypuff när den aktiveras. Den kallas för MDI (Pressurised Metered Dose Inhaler, pMDI) - i dagligt tal "spray" och är fortfarande den vanligaste typen av inhalationsaerosol i Europa, dock inte i Sverige där man allt mer gått över till pulverinhalatorer. När man i samband med freonförbudet utvecklade pulverinhalatorer (Dry Powder Inhaler, DPI) gick utvecklingen i många avseenden framåt. Det har även hela tiden funnits en parallell utveckling i de fristående aerosolgeneratorer, nebulisatorer, som kan användas med valfritt läkemedel i vätskeform vilka kan leverera större mängder läkemedel.
Deponeringsmönster för ett läkemedel i lungan
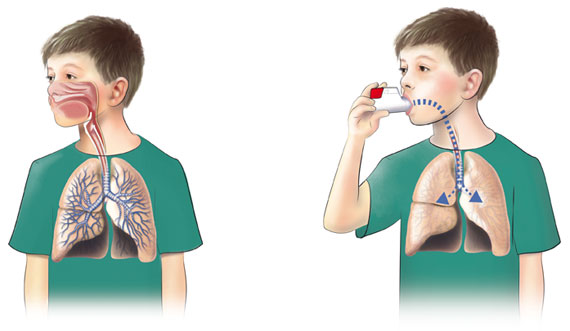
Deponering betyder att en partikel eller droppe i luftströmmen får kontakt med en yta och fastnar. Viktiga faktorer för en bra deponering är partikelns aerodynamiska diameter, andningsmönstret och luftvägarnas dimensioner. För att nå längst ut i lungan och dess alveoler måste luften (och eventuell aerosol) passera genom de övre luftvägarna, det vill säga munhåla, svalg och de nedre luftvägarna (trakea, bronker och bronkioler).
De nedre luftvägarna förgrenar sig i ungefär 20 gånger på vägen från trakea längst ut till alveolerna. En effekt av denna förgrening är att den sammanlagda tvärsnittsytan ökar kraftigt i längst ner i de små luftvägarna och att de flödesbegränsande luftvägarna ligger relativt tidigt. Det är således en relativt liten yta som är det huvudsakliga målet för de flesta av de läkemedel vi andas in vid behandling av luftvägssjukdomar som till exempel astma och KOL. Om vi talar om stora luftvägar (fram till nionde delningen) rör det sig för en vuxen om cirka 0,04 m2och om vi räknar ned till terminala bronkioler cirka 0,4 m2. Ytan står i kontrast till lungans alveolära del som är nere i alveolerna vars yta är flera hundra kvadratmeter.
- Med aerosol avses ett system bestående av två faser: dels en gas (luft), dels droppar eller partiklar som är så små att de kan sväva i gasen.
- De viktigaste deponeringsmekanismerna för normala läkemedelsaerosoler är impaktion och sedimentation. Impaktion innebär att en partikel av sin egen tröghet fortsätter rakt fram (när luftvägen svänger), når en yta och fastnar. Sedimentation innebär att en partikel tyngre än luft faller nedåt på grund av gravitationen.
- Deponering av inhalerad aerosol sker i huvudsak på tre olika ställen. Dessa är: A ) mun och svalg, B) nedre luftvägar (trakea och bronker) eller C) den alveolära delen.
Deponering av farmakologiska aerosoler sker i huvudsak på grund av impaktion, både i mun och svalg och i den trakeobronkiella delen av lungan. Impaktionen är beroende av partikelns hastighet. I den alveolära delen av lungan sker deponering genom sedimentation. Sedimentationen ökar med uppehållstiden och avståndet till närmaste yta. Såväl impaktion som sedimentation ökar med partikelns massa eller storlek. Både mun och svalg (och framför allt näsan) och den trakeobronkiella delen av lungan fungerar som ett filter för att skydda den ömtåliga alveolära delen av lungan. Partiklar filtreras ur luftströmmen, fastnar på slemhinnorna och transporteras till svalget med hjälp av den mukociliära transporten.
De faktorer vi kan påverka i form av partikelstorlek och inhalationshastighet avgör hur stor andel av den inhalerade aerosol som deponeras i den viktiga tracheobronkiella regionen. Deponeringen i den trakeobronkiella delen av lungan är koncentrerad till generation fyra till sju i luftvägsträdet, vilket är den flödesbegränsande regionen eftersom hastigheten på luftströmmen är störst här. Detta ger störst förutsättningar för impaktion.
I den alveolära delen påverkas även sedimentationshastigheten av partikelstorleken, men inte av inhalationsflödet. Uppehållstiden är relativt sett mycket lång och kan enkelt förlängas ytterligare genom att man håller andan. En stor andel av deponeringen som sedimentation i alveolerna är oftast inte någon fördel när det gäller att behandla luftvägarna.
- Deponering på grund av impaktion sker dels i mun och svalg, dels i de flödesbegränsande luftvägarna, den trakeobronkiella delen.
- Deponering i alveolerna sker genom sedimentation
Alltid en kompromiss
Det är normalt en stor skillnad i deponeringsmönster mellan individer, men för samma individ är mönstret rimligt reproducerbart. Inandningar av aerosol genom munnen är nästan alltid rätt utgångspunkt. Hög grad av deponering i de övre luftvägarna kan ge upphov till lokala biverkningar, till exempel i form av heshet vid inhalation av steroider, och bidrar inte heller nämnvärt till den kliniska effekten vid lungsjukdom. För att hålla deponeringen (som sker på grund av impaktion) på en låg nivå bör inhalationsflödet hållas lågt. Nästa fråga man måste ställa sig är hur man vill fördela aerosolen på de två återstående lokalisationerna, den trakeobronkiella delen och den alveolära delen av lungan.
Vi kan påverka fördelningen mellan dessa två områden, eftersom deponeringsmekanismerna är olika, men vi kan inte påverka deponeringsmönstret inom den trakeobronkiella delen (de nedre luftvägarna) speciellt mycket. I sammanställningar över läkemedel i olika sammanhang talas det ofta om deponering i små luftvägar och lika ofta är stödet scintigrafiska bilder från radioaktivt märkta inhalerade aerosoler. Upplösningen med den här typen av metoder är i förhållande till de minsta luftvägarnas storlek mycket dålig vilket kraftigt försvårar en bedömning om att avgöra om en partikel ligger alveolärt eller i de minsta luftvägarna (bronkiolerna). Det går inte heller att i humanförsök undersöka varje generation för sig för att till exempel undersöka hur mycket av en aerosol som har deponerats i den flödesbegränsande sjätte generationen i luftvägsträdet.
Det stöd därför som egentligen finns för att uppskatta deponeringsmönstret inom den trakeobronkiella regionen bygger på teoretiska modeller i kombination med empirisk validering. Det finns ett antal matematiska dataprogram där ingångsparametrarna är generell storlek av lungan, partikelstorlek och inhalationsflöde, vilka sedan beräknar deponeringen för varje givet segment/generation. När man summerar deponeringen för varje enskild generation i den trakeobronkiella delen av lungan stämmer resultaten från dessa teoretiska modeller mycket bra med empiriska data för deponering såväl i den trakeobronkiella delen som i den alveolära delen av lungan; detta oavsett vilka partikelstorlekar och inhalationsflöden som valts.
För att återknyta till deponeringsställena mun och svalg, trakea och bronker eller den alveolära delen kan vi alltså i viss mån påverka på vilket av dessa tre ställen vi deponerar partiklar. Vill vi deponera det mesta i mun och svalg är det lätt. Stora partiklar och högt inhalationsflöde löser detta. Vill vi deponera så mycket som möjligt i alveolerna är detta också relativt enkelt. Små partiklar och låga inhalationsflöden i kombination med att man håller andan ger mycket goda förutsättningar för deponering genom sedimentation i alveolerna. Mer besvärligt blir det när vi vill ha hög deponering i den trakeobronkiella delen. Det är nästan alltid dit vi vill styra inhalationsläkemedel i aerosolform. Stora partiklar och högt flöde ger mycket deponering genom impaktion, som om detta är förutsättningen när en aerosol kommer in i trakea är det hela löst. Problemet är dock att med dessa förutsättningar är även deponeringen i mun och svalg mycket hög och det blir en liten del av aerosolen som klarar sig förbi första den delen för att nå de nedre luftvägarna.
En sammanställning av en stor mängd experimentella data visar att man hos friska generellt inte kan deponera mer än 30 procent av en inhalerad aerosol i den trakeobronkiella regionen, nedre luftvägarna. Detta maximum vid ett normalt inhalationsflöde (0,5 L/sek) uppträder vid en partikelstorlek på cirka 6 μm alternativt ett högre inhalationsflöde om 1 L/sek och en 4 μm partikelstorlek.
Inhalatorer
Pulverinhalatorer
I Europa har inhalationsbehandling i länder som Sverige, Norge, Danmark och Nederländerna dominerats av pulverinhalatorer (dry powder inhaler, DPI). Dessa innehåller inte drivgaser eller konventionellt smörjmedel utan endast läkemedel eller läkemedel blandat med en bärarsubstans (till exempel laktos) för att förbättra aerosolens egenskaper. Internationellt och även i Sverige finns ett stort antal olika inhalatorer från endos till multidos, många med räkneverk. När läkemedelssubstansen hanteras i den farmaceutiska produktionen fylls inhalatorn med substanspartiklar som är betydligt större än de partiklar som senare skall andas in. I pulverinhalatorerna används den energi som skapas av inhalationsflödet (dvs. tryckfallet) för att dela upp (deaggregera) substansen till mindre partiklar.
Olika pulverinhalatorer kräver olika flöden för att fungera optimalt. Den slutgiltiga partikelstorleken och kvaliteten på den tillgängliga dosen blir därför beroende av inhalationen. Generellt kan man säga att vid låg inhalationsansträngning (lågt tryckfall och därmed liten tillförd energi) blir partiklarna större, medan en kraftigare inhalationsansträngning (stort tryckfall) deaggregerar partiklarna mer fullständigt. Sambandet är generellt och innebär också att inhalatorer med högt motstånd (vilket ger stort tryckfall och stor tillförd energi) vid optimal användning leder till ett aerosolmoln med mindre partiklar och därmed högre perifer deponering.
Vid behandling av barn och patienter med svår lungsjukdom bör man kontrollera att de orkar utföra det andningsarbete som krävs. Pulverinhalatorerna är olika känsliga för hur man håller dem i samband med att en ny dos laddas och att det angivna inhalationsflödet uppnås. Inhalationsflödets påverkan på den slutliga partikelstorleken är inte enbart en effekt av inhalatorns motstånd utan också av flödesegenskaperna för pulvret.
Dosaerosol, inhalationsspray, (pMDI = pressurised metered dose inhaler)
Den första bärbara inhalatorn kom 1956 och var en liten trycksatt, ventilförsedd metallbehållare (så kallad kanister) som levererade en fastställd dos vid varje avfyrningstillfälle. På engelska kallas de pMDI (pressurised metered dose inhalor) och svenska kallas den ofta för dosaerosol (eller "spray"). Dessa astmasprayer är billiga, robusta, relativt enkla att hantera och ser principiellt lika ut för flera olika sorters läkemedel. Läkemedlet finns i vätskan inuti den trycksatta behållaren. Ventilstorlek, koncentration av läkemedlet och i förekommande fall fördelningen av suspension i dosaerosolen är några av de faktorer som bestämmer avgiven dos från en dosaerosol och varje kombination av läkemedel, drivgaser och smörjmedel har unika egenskaper. Äldre tiders dosaerosoler använde drivgaser av freontyp och genererade ofta relativt stora partiklar med en mycket hög utgångshastighet, vilket innebar att en stor del av dosen deponerades på slemhinnan i mun och svalg. Lungdeponeringen var för dessa pMDI regelmässigt mindre än 20 procent och inte sällan mindre än 10 procent. När man introducerade nya drivgaser av typen HFA (hydrofluoroalkan), som är mindre skadliga för miljön, utvecklades också dos-aerosolerna så att utgångshastigheten för partiklarna som tidigare kunde vara så hög som 30 m/sek har minskades väsentligt.
Utgångshastigheten av spraymolnet kan ställa till en del problem med oönskad deponering och det är därför, generellt sett, viktigt att koordinera avfyrandet av en pMDI med andningen så att man fyrar av aerosolmolnet i början av inhalationen för att effekten skall bli optimal. Detta har visat sig svårt för många. Koordinationsproblem har framhållits som kanske den största nackdelen med dosaerosoler. För läkemedel i suspensionsform gäller fortsatt att dropparna/partiklarna är större och läkemedelspartiklarna sedimenterar i kanistern. Dosaerosolen måste därför skakas ordentligt omedelbart före användning.
En annan nackdel med sprayer är att inhalation av smörjmedel och drivgaser kan orsaka hosta och sammandragning av luftvägarna hos enstaka patienter. En begränsning med många dosaerosoler är avsaknad av räkneverk och det kan upplevas som en begränsning att inte veta hur många doser som finns kvar.
Spacer eller inhalationsbehållare
För pMDI har deponeringen i mun och svalg varit hög och andelen aerosol som passerar stämbanden varit låg. Genom att kombinera dosaerosoler med olika former av inhalationsbehållare (spacer) mellan munhålan och inhalatorn kan systemet optimeras. En spacer har två principiella effekter. Den ena är att den kan minska munhåledeponeringen, särskilt för inhalatorer med stora droppar och hög utgångshastighet. Partiklar som annars skulle fastna i mun och svalg impakterar då istället i spacern. Den andra fördelen med spacer är att den minskar kraven på koordination, vilket kan vara en stor fördel då koordination eller medverkan inte är optimal, vilket kan leda till ökad deponering i nedre luftvägar och alveoler. Till detta kommer spacerns funktion som behållare för aerosolen så att drivgasen hinner dunsta bort, vilket kan minska droppstorleken. Därtill kommer möjligheten att använda lågt inhalationsflöde från spacern.
Val av inhalator/inhalationssystem
Man kan först konstatera att de nya läkemedlen för astma har medfört stora fördelar och kostnader för sjukhusvården av patienter med astma har minskat dramatiskt. Metoder för att utveckla följsamhet till en viss behandling behöver dock utvecklas vidare. Det finns klara skillnader mellan olika inhalationssystem. Många av inhalatorerna som finns tillgängliga är väl fungerande, och det gäller att välja ett som är tillräckligt bra och som patienten kan använda utan att göra små eller stora fel. Det är viktigt att komma ihåg att det är själva aerosolen ("dimman") - och därmed inhalatorns konstruktion - och inhalationsmönstret som bestämmer hur läkemedlet deponeras.
Om två aerosoler är lika i fråga om partikel/droppstorlek och koncentration av dessa partiklar i luften är lika så torde alltså resultatet vid inhalation bli detsamma oavsett genereringsmekanism i olika inhalatorer. Det är också svårt att på kliniska grunder konstatera att pulverinhalatorer generellt skulle vara bättre än pMDI. Det är med stor sannolikhet en väsentlig fördel att använda inhalatorer som ger god återkoppling till patienten och även till förälder med mindre barn avseende till exempel att rätt flöde uppnåtts, att en dos har avgivits, och att det finns läkemedel kvar i inhalatorn.
Nebulisering kan användas för att leverera stora mängder läkemedel. Om ventilationen är ojämn som till exempel vid KOL kan det sannolikt vara en fördel att dosen fördelas över flera andetag. Nackdelarna är att behandlingen tar längre tid, att det krävs dyrare utrustning och att utrustning bör kontrolleras och underhållas regelbundet.
En svaghet med inhalationsbehandling jämfört med exempelvis peroral behandling kan vara att den upplevs som tekniskt komplicerad och att det finns många olika utrustningar att hålla rätt på. Det finns dock bra system att tillgå och ofta finns flera alternativ. För lyckat resultat är det angeläget att såväl behandlare som patient kan hantera den aktuella utrustningen. Därutöver finns det skäl att systematiskt utvärdera effekterna av sin insatta behandling. Vid utebliven effekt är det sannolikt att man använder läkemedel på fel indikation eller att patienten inte använder inhalatorn rätt. Det är därför viktigt att välja en inhalator som patienten tycks föredra och kan hantera, samt att regelbundet kontrollera inhalationstekniken.
En sammanfattning
Sammanfattningsvis har alltså pulverinhalatorerna en rad fördelar som den automatiska synkroniseringen mellan inhalationen och genereringen av aerosolen, liksom att läkemedlet i många fall kan användas utan andra ämnen som konserveringsmedel, oljor och drivmedel. Många flerdosinhalatorer av pulvertyp har dessutom inbyggt räkneverk och en del återkopplingsfunktioner för genomförd inhalering. Till nackdelarna hör att aerosolens kvalitet och dosstorlek är beroende av en korrekt inhalation och att dosen vid felaktig användning kanske inte ens lämnar inhalatorn. Själva apparaten innehåller fler rörliga delar och är dyrare att tillverka än en pMDI.

Nyhetsbrev från Viatris
Prenumerera på Viatris nyhetsbrev och ta del av nyheter, information och utbildningar. Nyhetsbrevet sammanställs och distribueras av Viatris.